علت استفاده از بازدارنده های شعله در پلیمرها

معدنی:
هر نوع پرکننده غیر آلی، حتی خنثی، میتواند به چند دلیل در واکنش پلیمرها با آتش مؤثر باشد:
- میزان محصولات قابلاحتراق را کاهش میدهد
- شرایط برای قابلیت هدایت گرمایی ماده ایجاد میشود و خواص فیزیکی ماده را اصلاح میکند
- میزان گرانروی ماده را تغییر میدهد.
تمامی اتفاقات ذکرشده میتواند در عملکرد آتش گرفتن پلیمرها مداخله کند. بااینحال، بعضی از مواد معدنی بهعنوان تأخیر انداز شعله، به علت رفتاری که در دماهای بالا دارند، شناختهشدهاند.
متداولترین تأخیراندازهای شعله هیدروکسیدهای فلزی، هیدروکسی کربناتها و بوراتهای روی هستند. در کنار تأثیرات ذکرشده، این افزودنیهای غیر آلی یک واکنش تأخیر انداز شعله فیزیکی مستقیم نیز دارند. زمانی که دما افزایش مییابد، این پرکنندهها بهصورت گرماگیر تخریب میشوند؛ بنابراین انرژی فرایند را جذب میکنند. این نوع تأخیراندازها، مولکولهای غیرقابل اشتعال (H2O,CO2) منتشر میکنند که گازهای قابلاحتراق را رقیق کرده و یکلایه محافظ سرامیکی یا شیشهای ایجاد میکنند.
هیدروکسیدهای فلزی:
هیدروکسیدهای فلزی بهصورت گرماگیر تخریب میشوند و در دمایی بالاتر از محدوده دمایی فرآیند پلیمر و در حدود دمای تخریب پلیمر آب منتشر میکنند. دو نوع متداول از این تأخیراندازهای شعله منیزیمدیهیدروکساید (MDH) و آلومینیوم تری هیدروکساید (ATH) است.
هیدروکسیکربناتها:
اکثر کربناتها در دمای بالا CO2 آزاد میکنند بهجز کربناتهای منیزیم و کلسیم که در دمای کمتر از 1000 درجه سانتیگراد گاز CO2 آزاد میکنند. درهرصورت، هیدورکسی کربناتها نسبت به سایر تأخیراندازهای متداول کمتر استفاده میشوند
بورات ها:
بوراتها نوع دیگری از خانوادههای افزودنی غیر آلی با خواص تأخیراندازی شعلهاند که در بین آنها بوراتهای روی مثل 2ZnO.3B2O3.3H2O بیشتر استفاده میشوند. محصولات تخریب گرمایی آنها اکسید بور و اسید بوریک است که منجر به تشکیل یکلایه محافظ شفاف میشود. درصورتیکه پلیمر موردنظر شامل اکسیژن باشد، حضور اسید بوریک باعث هیدروژنزدایی شده و درنتیجه یکلایه کربنی شکل میگیرد. پرمصرفترین ترکیب اسید بوریک است. اسید بوریک و بورات سدیم (بوراکس Na2 B4 O7.10H2O) دو ماده تأخیر انداز شعله هستند که اصولاً برای مواد سلولزی مورداستفاده قرار میگرفتند.
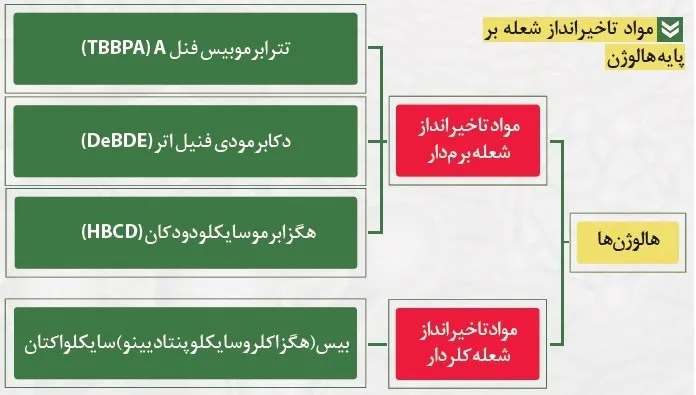
هالوژنها:
برم و کلر به علت انرژی پیوندکمی که با اتمهای کربن دارند، میتوانند در فرآیند سوختن حضورداشته باشند. یک سازوکار برای بهبود تأخیراندازی شعله مواد ترموپلاستیک، کاهش نقطۀ ذوب آنها است. نتیجه این امر در نحوة تشکیل بازدارندههای رادیکالهای آزاد در آتش است و سبب دور شدن ماده از شعله بدون سوختن آن میشود. بازداشتن رادیکالهای آزاد موجب کاهش گازهای سوختنى تولیدشده در اثر سوختن ماده میشود. حرارت مواد سوختنى، موجب تشکیل رادیکالهای هیدروژن، اکسیژن، هیدروکسید و پروکسید که متعاقباً توسط آتش اکسیدشده، میشود. مواد تأخیر انداز شعله این رادیکالها را به دام میاندازند و درنتیجه از اکسیدشدنشان جلوگیری میکنند. هالوژنهای برم یا کلر میتوانند بهعنوان پوششی از گازهای محافظ و برای رقیق کردن گازهای سوختنی موردتوجه قرار بگیرد. علاوه بر این مواد مذکور میتوانند موجب تسریع اکسایش فاز جامد شود و با توجه به اینکه محصولات اکسایش تمایل دارند به اینکه بهصورت حلقوی باشند، یکلایه جامد محافظ ایجاد میشود. از طرف دیگر X● نسبت به H• و OH• واکنشپذیری کمتری دارند. مونومرها و کوپلیمرهای هالوژنی (تاخیراندازهای شعله واکنشی)- ازجمله مزایای مونومرها و کوپلیمرهای تأخیر انداز شعله واکنشی این است که به علت حضور در داخل زنجیره و ساختار پلیمر میتوانند در غلظتهای پایین مورداستفاده قرار گیرند؛ امتزاجپذیری را بین پلیمر و عامل تأخیر انداز شعله افزایش میدهند؛ آسیبهایی که در اثر افزودنیهای ناهمگن بر خواص مکانیکی اعمال میشود را محدود میکنند و مهاجرت عاملهای تأخیر انداز شعله به سمت سطح کاهش مییابد . بااینحال، این دسته از تأخیراندازها نیاز به یک مرحله افزودن به ساختار دارند که برای استفاده در صنعت مناسب نخواهد بود. واکنش این محصولات بسیار شبیه تأخیراندازهای شعله افزودنی است .آنها با ذرات بسیار فعال H• و OH•واکنش میدهند و واکنش تخریب را متوقف میکنند.(نظیر پارافینهای کلردار، هالوفسفاتها، ترکیبات آروماتیک برمدار مانند تریبرموتولوئن و پنتابرموفنیلآلیلاتر)
آنتیموآن:
تنها در حضور هالوژنها عمل میکند. همانند فسفرها برای جمعآوری رادیکالهای آزاد هیدروژن و هیدروکسید که برای سوختن لازم هستند، عمل میکند. در آتش، هالیدهای آنتیموآن و هالید اکسیدها در حجمهای کافی تولید میشوند که درنتیجه آن پردهای مهمانند از گاز خنثی بر روی جسم ایجاد میشود که از رسیدن اکسیژن به سطح جسم و همچنین گسترش شعله جلوگیری میکند.
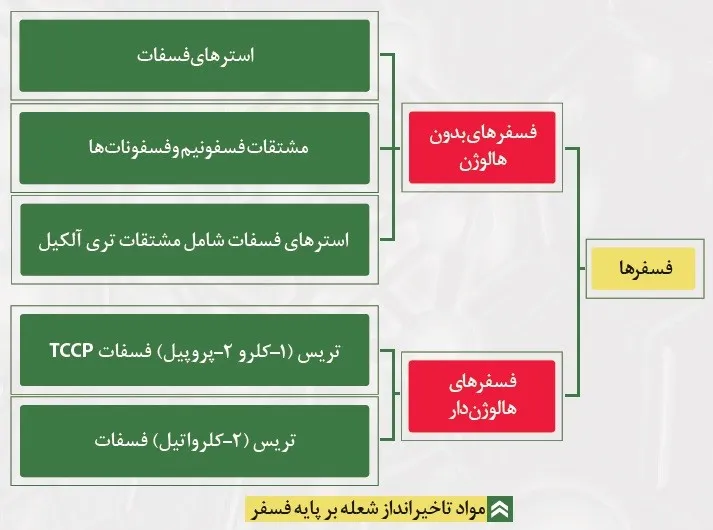
فسفرها:
فسفرها با ایجاد خاکستر که بهصورت تشکیل اسید فسفریک و کاهش رهایش بخارات قابل اشتعال است، عمل میکنند.
محدوده محصولات تأخیر انداز شعله بر پایه فسفرها بسیار گسترده است که این محدوده شامل فسفاتها، فسفناتها، فسفیناتها، اکسیدهای فسفین و فسفر قرمزها میشود. این مواد میتوانند بهصورت افزودنی و یا با حضور در زنجیره پلیمر استفاده شوند و در فاز متراکم و بخار فعال باشند اساساً تأخیراندازهای شعله بر پایه فسفر در فاز متراکم، برای پلیمرهایی که شامل اکسیژناند، (پلیاسترها، پلیآمیدها، سلولز و ...) بهطور مؤثر عمل میکنند. تخریب گرمایی در حضور این مواد اسید فسفریک تولید میکند سپس این ماده متراکم شده و پیروفسفات همراه با آب تولید میکند که این آب باعث رقیقشدن فاز گاز اکسیدکننده میشود.
علاوه بر این، اسید فسفریک و اسید پیروفسفریک میتوانند واکنش آبزدایی الکلهای انتهایی را سرعت بخشند و این واکنش پیوندهای دوگانه کربوکاتیونی و کربن-کربن ایجاد میکند. در دماهای بالا اتصالهای عرضی و ساختارهای کربنی ایجاد میشود و اسید ارتو و پیروفسفریک به متافسفریک و پلیمرهای مشابه (PO3H)n تبدیل خواهند شد.
آنیونهای فسفات (پیرو و پلیفسفاتها) در تشکیل زغال باقیمانده کربنی مشارکت میکنند. این لایه محافظ کربنی پلیمر را ایزوله کرده و تماس آن را با شعلهها متوقف میکند؛ فراریت سوخت را محدود کرده و از تشکیل رادیکالهای آزاد جدید جلوگیری میکند؛ نفوذ اکسیژن را محدود میکند و درنتیجه سوختن کاهش مییابد و پلیمر زیرین را نسبت به حرارت عایق میکند.
تأخیراندازهای شعله بر پایه فسفر بهشدت در پلیمرهای شامل نیتروژن و اکسیژن مؤثرند. درصورتیکه در پلیمر موردنظر اکسیژن و یا نیتروژن وجود نداشته باشد ، باید از ، کمک افزودنیهایی مانند پلیالها، ازجمله پنتااریتویتول استفاده شود.
فسفرهای قرمز:
فسفرهای قرمز بیشترین مصرف را در بین تأخیراندازهای شعله بر پایه فسفر دارند و با غلظت کمی (کمتر از 10%) در مواد پلیمری استفاده میشوند. این نوع تأخیراندازهای شعله در پلیمرهایی مانند پلیآمیدها و پلییورتانها بسیار مؤثرند. بههرحال، سازوکار عملکرد آنها هنوز بهصورت واضح مشخص نشده است.فسفاتهای غیر آلی- آمونیوم پلی فسفات (APP) یک نمک غیر آلی از اسید پلی فسفریک و آمونیاک است. طول زنجیره (n) برای این ترکیبات پلیمری و همچنین تعداد شاخه برای این پلیمرها متفاوت است.
تاخیراندازهای بر پایه فسفر آلی- این ترکیبات شامل ارگانوفسفرها، فسفاتاسترها، فسفاتها و فسفیناتها هستند. ازجمله میتوان از تری فنیل فسفات (TPP) نام برد که در پلاستیکهای مهندسی استفاده میشود.
[نظیر تریکرزیلفسفات (TCP) و تریآریلفسفات (TAP)]
سامانههای بازدارنده شعله فوم کننده- فوم بهمحض تشکیل یکلایه کربنی بر روی سطح پلیمر در طول تخریب گرمایی به وجود میآید. این لایه بهعنوان یک سد نارسانا عمل میکند و انتقال گرما را بین منبع گرمایی و سطح پلیمر کاهش میدهد. همچنین، انتقال سوخت را از سمت پلیمر به سمت شعله و نفوذ اکسیژن را در ماده کاهش میدهد. بیشترین منبع اسیدی استفادهشده در این ترکیبات آمونیوم پلیفسفات (APP) است که در پلیالفینها به حضور یک عامل کربنی مانند پنتااریتریتول نیز نیاز است.
نیتروژن
نیتروژن بهعنوان یک افزایشدهنده تأخیراندازی شعله به همراه فسفر و همچنین بهتنهایی در پلیآمیدها و آمینوپلاستها، شناخته میشود. اصولاً مواد تأخیر انداز شعله نیتروژنی در پلیمرهای نیتروژندار نظیر پلییورتانها و پلیآمیدهاست. ملامین یک محصول بلورین است که دارای 67% وزنی اتمهای نیتروژن است. این ماده در دمای 350 درجه سانتیگراد تصعید و در دمای 345 درجه سانتیگراد ذوب میشود. بهمحض تصعیدشدن مقدار بالایی انرژی جذب کرده و دما را کاهش میدهد. ملامین در دمای بالا با حذفشدن آمونیاک تخریب میشود و اکسیژن و گازهای قابلاحتراق را رقیق کرده یکلایه متراکم و پایدار در مقابل حرارت ایجاد میکند که درون آن ملام، ملیم و ملون وجود دارد. عملکرد نمکهای ملامین در فاز متراکم بهطور فراوانی بالاتر است. علاوه بر این، ترکیباتی چون فسفات ملامین تخریب گرماگیری دارند که منجر به تشکیل ملامین پلی فسفات و رهاسازی ملامین و اسید فسفریک میشود. اسید فسفریک آزادشده خواصی مشابه تأخیراندازهای شعله بر پایه فسفر دارد. ملامین پیروفسفات، در طول تخریب گرمایی، ملامین رها میکند، اما عملکرد گرمایی آن نسبت به ملامین و دیگر نمکها متفاوت است.
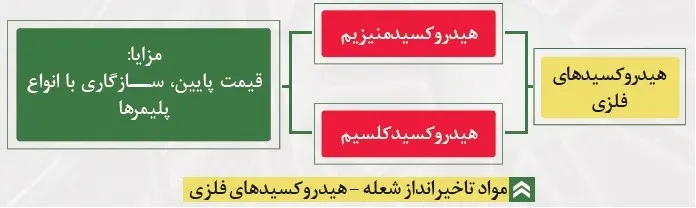
هیدروکسیدهای فلزی
سازوکار عمل: جذب حرارت، تولید آب، خن کردن آتش و پلیمر، رقیق کردن مخلوط گازهای قابل اشتعال.
سیلیکونها
اساساً افزودن مقدار نسبتاً کمی از ترکیبات سیلیکونی (سیلیکاها، سیلیکونها، سیلیکاتها، ارگانوسیلانها، سیلسکویی اکسانها و...) خاصیت تأخیراندازی شعله را در پلیمرها افزایش میدهد سیلیکونها، بهعنوان موادی با پایداری حرارتی و مقاومت حرارتی بالا، با رهایی مقدار بسیار کمی گازهای سمی در طول تخریب گرمایی شناختهشدهاند. رفتار خوب مشتقات سیلیکونی بهعنوان تأخیر انداز شعله به علت بخش آلی آنها در پلیکربنات و مهاجرت بهسوی سطح در طول سوختن ماده است که نتیجه آن ایجاد یک زغال مقاوم در برابر آتش است که از ترکیبات سیلوکسان و ترکیبات آروماتیک متراکم به دست میآید.
نانوذرات
ذرات نانومتری بهعنوان موادی که خواصی نظیر مقاومت گرمایی، استحکام مکانیکی و مقاومت در برابر سوختن را در پلیمر افزایش میدهند، شناختهشدهاند. اساساً بسته به ساختار شیمیایی و شکل هندسی ذرات نانو، قابلیت تأخیراندازی شعله آنها در پلیمر متفاوت خواهد. بود. نانورسها، نانولولههای کربن، نانوذرات اکسید فلزی، نانوذرات کروی سیلیکات، سیلسکوئیاکسان و ذرات متالیک اکساید خواص تأخیراندازی شعله خوبی را از خود نشان میدهند. بهمحض حرارت دادن و افزایش دما، گرانروی مذاب نانوکامپوزیت پلیمر کاهش مییابد و نانوذرات به سمت سطح ماده مهاجرت میکند. جمع شدن نانوذرات بر سطح مواد بهعنوان مانع محافظ عمل میکند و انتقال حرارت به ماده، فراریت محصولات تخریبی سوختن و نفوذ اکسیژن به درون ماده را محدود میکند.
متأسفانه استفاده از دیرسوزکنندهها در پلیمرها به علت اینکه تلفات حاصله از آتشسوزی اکثراً به خاطر محصولات سمی ناشی از دود هست، پیچیده هست و لذا راهحلهای دیگری را الزامی نموده است. از این دسته میتوان به استفاده از مواد پفکی شکل که در زمان گرم شدن متورم شده و ماده قابلاحتراق را از آتش و اکسیژن دورنگه میدارد، اشاره نمود. روش دیگر سعی در توسعه پلیمرهایی نظیر رزینهای فنولی است که با تبدیلشدن به زغالی سخت در حین سوختن، مواد قابلاحتراق زیرین را محافظت نمایند.